-
Lớp 12
-
Lớp 11
-
Lớp 10
- SGK Toán 10 - Đại Số và Hình Học Toán 10
- SGK Toán 10 nâng cao
- SGK Tiếng Anh 10
- SGK Tiếng Anh 10 Mới
- Văn mẫu 10
- Soạn văn 10 chi tiết
- Soạn văn 10 ngắn gọn
- Soạn văn 10 siêu ngắn
- Tác giả - Tác phẩm văn 10
- SGK Vật lý 10
- SGK Vật lý 10 nâng cao
- SGK Hóa học 10
- SGK Hóa học 10 nâng cao
- SGK Sinh học 10
- SGK Sinh học 10 nâng cao
-
Lớp 9
-
Lớp 8
-
Lớp 7
-
Lớp 6
- Lớp 5
- Lớp 4
- Lớp 3
- Lớp 2
- Lớp 1
- Thông tin tuyển sinh
Câu hỏi 1
Đáp án đúng:
Đáp án A
Câu hỏi:
Cho x gam Al tan hoàn toàn vào y mol HCl thu được dung dịch Z chứa 2 chất tan có cùng nồng đô mol. Thêm từ từ dung dịch NaOH vào dung dịch Z thì đồ thị biểu diễn lượng kết tủa phụ thuộc vào lượng OH- là:
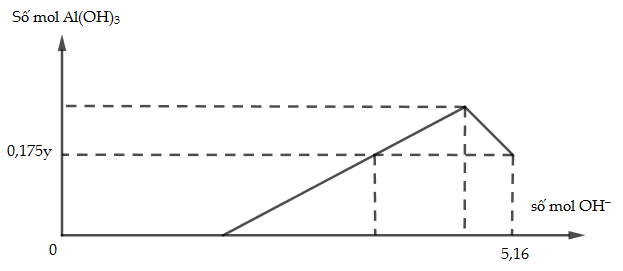
Giá trị của x là:
Phương pháp giải :
Bài toán muối nhôm tác dụng với dd kiềm
Các phản ứng xảy ra:
Al3+ + 3OH-→ Al(OH)3 (1)
Al(OH)3 + OH-→ [Al(OH)4]- (2)
Từ (1) và (2) ta rút ra kết luận:
+ Nếu b/a ≤ 3 thì kết tủa chưa bị hoà tan và
nAl(OH)3= b/3
+ Nếu 3 < b/a < 4 thì kết tủa bị hoà tan 1 phần
Al3+ + 3OH-→ Al(OH)3 (1)
mol a →3a →a
Al(OH)3 + OH- → [Al(OH)4]- (2)
Mol b-3a b-3a
nAl(OH)3= 4a-b
+ Nếu b/a ≥ 4 thì kết tủa bị hoà tan hoàn toàn
Lời giải chi tiết :
Vì Z có 2 chất tan cùng nồng độ mol => đó là AlCl3 và HCl
=> nAlCl3 = nHCl => n = y – 3n => y = 4n (1)
Tại nOH = 5,16 mol thì kết tủa tan 1 phần
=> nAl(OH)3 = 4nAl3+ - (nOH – nHCl (Z) )
=> 0,175y = 4n – ( 5,16 – n) (2)
Từ (1,2) => n = 1,2 mol
=> x = 32,4g
Đáp án A
Đáp án A:
32,40
Đáp án B:
26,10
Đáp án C:
27,00
Đáp án D:
20,25


