-
Lớp 12
-
Lớp 11
-
Lớp 10
- SGK Toán 10 - Đại Số và Hình Học Toán 10
- SGK Toán 10 nâng cao
- SGK Tiếng Anh 10
- SGK Tiếng Anh 10 Mới
- Văn mẫu 10
- Soạn văn 10 chi tiết
- Soạn văn 10 ngắn gọn
- Soạn văn 10 siêu ngắn
- Tác giả - Tác phẩm văn 10
- SGK Vật lý 10
- SGK Vật lý 10 nâng cao
- SGK Hóa học 10
- SGK Hóa học 10 nâng cao
- SGK Sinh học 10
- SGK Sinh học 10 nâng cao
-
Lớp 9
-
Lớp 8
-
Lớp 7
-
Lớp 6
- Lớp 5
- Lớp 4
- Lớp 3
- Lớp 2
- Lớp 1
- Thông tin tuyển sinh
Bài 7 trang 138 SGK Hóa học 11
Đề bài / Mô tả:
Xem lời giải và đáp án chi tiết cho bài 7 trang 138 SGK Hóa học 11
Đề bài
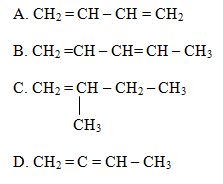
Đốt cháy hoàn toàn 5,40g ankadien liên hợp X thu được 8,96 lít khí CO2 (đktc) Công thức nào sau đây là công thức cấu tạo của X ?
Phương pháp giải - Xem chi tiết
Gọi công thức phân tử của ankadien liên hợp là CnH2n-2 ( n ≥ 4)
Tính số mol của CO2
BTKL => mH = mX – mC =? => nH2O= ?
Đốt cháy X luôn có: nX = nCO2 – nH2O =? (mol) (Vì X có 2 liên kết pi trong phân tử)
\(n = \frac{{{n_{C{O_2}}}}}{{{n_X}}} = ?\) => CTPT và CTCT của X
Lời giải chi tiết
Gọi công thức phân tử của ankadien liên hợp là CnH2n-2 ( n ≥ 4)
Ta có: \({n_{C{O_2}}} = \dfrac{{8,96}}{{22,4}} = 0,4\,\,mol\)
\( \to {n_C} = {n_{C{O_2}}} = 0,4\,\,mol \to {m_C} = 0,4.12 = 4,8\,\,gam\)
\( \to {m_H} = 5,4 - 4,8 = 0,6\,\,gam\)
\( \to {n_H} = \dfrac{{{m_H}}}{1} = \dfrac{{0,6}}{1} = 0,6\,\,mol\)
\( \to {n_{{H_2}O}} = \dfrac{1}{2}{n_H} = \dfrac{1}{2}.0,6 = 0,3\,\,mol\)
Đốt cháy ankađien ta có: \({n_{ank{\rm{ađ}}ien}} = {n_{C{O_2}}} - {n_{{H_2}O}} = 0,4 - 0,3 = 0,1\,\,mol\)
\( \to số\,\,C = n = \dfrac{{{n_{C{O_2}}}}}{{{n_{anka{\rm{đ}}ien}}}} = \dfrac{{0,4}}{{0,1}} = 4\)
Vậy CTPT của X là C4H6
Vì X là ankađien liên hợp nên CTCT của X là CH2=CH-CH=CH2
Đáp án A


