-
Lớp 12
-
Lớp 11
-
Lớp 10
- SGK Toán 10 - Đại Số và Hình Học Toán 10
- SGK Toán 10 nâng cao
- SGK Tiếng Anh 10
- SGK Tiếng Anh 10 Mới
- Văn mẫu 10
- Soạn văn 10 chi tiết
- Soạn văn 10 ngắn gọn
- Soạn văn 10 siêu ngắn
- Tác giả - Tác phẩm văn 10
- SGK Vật lý 10
- SGK Vật lý 10 nâng cao
- SGK Hóa học 10
- SGK Hóa học 10 nâng cao
- SGK Sinh học 10
- SGK Sinh học 10 nâng cao
-
Lớp 9
-
Lớp 8
-
Lớp 7
-
Lớp 6
- Lớp 5
- Lớp 4
- Lớp 3
- Lớp 2
- Lớp 1
- Thông tin tuyển sinh
Trang chủ » 55 câu hỏi lý thuyết mức độ thông hiểu về tính chất - dãy điện hóa của kim loại có đáp án và lời giải chi tiết
55 câu hỏi lý thuyết mức độ thông hiểu về tính chất - dãy điện hóa của kim loại có đáp án và lời giải chi tiết
Lớp:
Môn học:
Bài học:
Bài 18. Tính chất của kim loại. Dãy điện hoá của kim loại
Câu trắc nghiệm:
Câu hỏi 1
Đáp án đúng:
Đáp án B
Câu hỏi:
Khi cho mẫu Zn vào bình đựng dung dịch X, thì thấy khối lượng chất rắn trong bình tăng lên. Dung dịch X là:
Lời giải chi tiết :
Đáp án B
Đáp án A:
Cu(NO3)2.
Đáp án B:
AgNO3.
Đáp án C:
KNO3.
Đáp án D:
Fe(NO3)3.
Câu hỏi 2
Đáp án đúng:
Đáp án C
Câu hỏi:
Cho hỗn hợp gồm Fe và Mg vào dung dịch AgNO3 khi các phản ứng xảy ra hoàn toàn thu được dung dịch X (gồm 2 muối) và chất rắn Y ( gồm 2 kim loại ) . 2 muối trong X là :
Lời giải chi tiết :
(1) Mg + 2Ag+ → Mg2+ + 2Ag
(2) Fe + 2Ag+ → Fe2+ + 2Ag
(3) Fe2+ + Ag+ → Fe3+ + Ag
Vì Chất rắn Y gồm 2 kim loại => đó là Ag và Fe => không thể xảy ra (3) và Ag+ phải hết
=> X gồm Mg2+ và Fe2+
Đáp án C
Đáp án A:
Fe(NO3)3 và Mg(NO3)2
Đáp án B:
AgNO3 và Mg(NO3)2
Đáp án C:
Mg(NO3)2 và Fe(NO3)2
Đáp án D:
Mg(NO3)2 và Fe(NO3)2
Câu hỏi 3
Đáp án đúng:
Đáp án B
Câu hỏi:
Cho hỗn hợp gồm Zn và Fe vào dung dịch CuSO4, phản ứng xong thu được chất rắn X gồm 2 kim loại và dung dịch Y chứa 3 loại ion. Nhận xét nào sau đây là đúng :
Lời giải chi tiết :
Thứ tự phản ứng :
Zn + Cu2+ -> Zn2+ + Cu
Fe + Cu2+ -> Fe2+ + Cu
=> chất rắn gồm 2 kim loại : Cu và Fe
Y chứa 3 ion là Zn2+ ; Fe2+ và SO42-.
=> Zn phản ứng hết, Fe còn dư, CuSO4 hết
Đáp án B
Đáp án A:
Zn chưa phản ứng hết, Fe chưa phản ứng, CuSO4 đã phản ứng hết
Đáp án B:
Zn đã phản ứng hết, Fe còn dư, CuSO4 đã phản ứng hết
Đáp án C:
Zn đã phản ứng hết, Fe phản ứng hết, CuSO4 còn dư
Đáp án D:
Zn đã phản ứng hết, Fe chưa phản ứng, CuSO4 đã phản ứng hết
Câu hỏi 4
Đáp án đúng:
Đáp án C
Câu hỏi:
Cho các phản ứng sau:
Fe + Cu2+→ Fe2+ + Cu;
2Fe2+ + Cl2→ 2Fe3+ + 2Cl-;
2Fe3+ + Cu → 2Fe2+ + Cu2+
Dãy chất và ion nào sau đây được sắp xếp theo chiều giảm dần tính oxi hóa?
Lời giải chi tiết :
Những phản ứng hóa học luôn có xu hướng tạo thành chất khử hoặc chất oxi hóa yếu hơn những chất ban đầu.
Fe + Cu2+→ Fe2++ Cu => Tính oxi hóa Fe2+< Cu2+
2Fe2++ Cl2 → 2Fe3++ 2Cl- => Tính oxi hóa Fe3+ < Cl2
2Fe3++ Cu → 2Fe2++ Cu2+ => Tính oxi hóa Cu2+ < Fe3+
Như vậy ta có sự so sánh về tính oxi hóa:
Cl2 > Fe3+ > Cu2+ > Fe2+
Đáp án C
Đáp án A:
Cu2+, Fe3+, Cl2, Fe2+
Đáp án B:
Fe3+, Cl2, Cu2+, Fe2+
Đáp án C:
Cl2, Fe3+, Cu2+, Fe2+
Đáp án D:
Cl2, Cu2+, Fe2+, Fe3+
Câu hỏi 5
Đáp án đúng:
Đáp án A
Câu hỏi:
Cho phương trình hóa học của phản ứng sau:
Fe + CuSO4 → FeSO4 + Cu
Phát biểu nào sau đây đúng?
Lời giải chi tiết :
A đúng
B sai vì Fe có tính khử mạnh hơn Cu
C sai vì Ion Cu2+ có tính oxi hoá mạnh hơn ion Fe2+.
D sai
Đáp án A
Đáp án A:
Ion Cu2+ có tính oxi hoá mạnh hơn ion Fe2+.
Đáp án B:
Kim loại Cu có tính khử mạnh hơn kim loại Fe.
Đáp án C:
Ion Fe2+ có tính oxi hoá mạnh hơn ion Cu2+.
Đáp án D:
Kim loại Cu khử được ion Fe2+
Câu hỏi 6
Đáp án đúng:
Đáp án A
Câu hỏi:
Ngâm thanh Cu dư vào dung dịch AgNO3 thu được dung dịch X. Sau đó ngâm thanh Fe dư vào dung dịch X thu được dung dịch Y. Biết các phản ứng xảy ra hoàn toàn. Dung dịch Y có chứa chất tan là:
Lời giải chi tiết :
![]()
Đáp án A
Đáp án A:
Fe(NO3)2
Đáp án B:
Fe(NO3)2; Cu(NO3)2.
Đáp án C:
Fe(NO3)3
Đáp án D:
Fe(NO3)3; Fe(NO3)2.
Câu hỏi 7
Đáp án đúng:
Đáp án A
Câu hỏi:
Bột Ag có lẫn tạp chất là Fe, Cu và Pb. Muốn có Ag tinh khiết, người ta ngâm hỗn hợp vào một lượng dư dung dịch X, sau đó lọc lấy Ag. Dung dịch X là:
Lời giải chi tiết :
Đáp án A
Đáp án A:
AgNO3.
Đáp án B:
HCl.
Đáp án C:
NaOH.
Đáp án D:
H2SO4.
Câu hỏi 8
Đáp án đúng:
Đáp án A
Câu hỏi:
Cho các kim loại: Na, Al, Fe, Pb, Cu, Ag. Số kim loại tác dụng với Fe(NO3)3 trong dung dịch?
Lời giải chi tiết :
Kim loại tác dụng trực tiếp với Fe(NO3)3 là : Mg , Al , Fe , Cu , Pb
Na tác dụng với H2O trước sau đó tạo NaOH mới tác dụng với Fe(NO3)3
Đáp án A
Đáp án A:
5
Đáp án B:
4
Đáp án C:
6
Đáp án D:
3
Câu hỏi 9
Đáp án đúng:
Đáp án C
Câu hỏi:
Cho các phản ứng xảy ra sau đây: (1) AgNO3 + Fe(NO3)2 → Fe(NO3)3 + Ag↓ (2) Mn + 2HCl → MnCl2 + H2↑Dãy các ion được sắp xếp theo chiều tăng dần ính oxi hóa là:
Phương pháp giải :
Theo nguyên tắc anpha :
Lời giải chi tiết :
Đáp án C
Đáp án A:
Ag+, Mn2+, H+, Fe3+
Đáp án B:
Mn2+, H+, Ag+, Fe 3+
Đáp án C:
Mn2+, H+, Fe3+, Ag+
Đáp án D:
Ag+, Fe3+, H+, Mn2+
Câu hỏi 10
Đáp án đúng:
Đáp án D
Câu hỏi:
Cho 2 phương trình rút gịn sau :
Fe + Cu2+ -> Fe2+ + Cu
Cu + 2Fe3+ -> Cu2+ + 2Fe2+
Nhận xét nào dưới đây đúng :
Lời giải chi tiết :
Các phương trình phản ứng đã cho liên quan đến các cặp oxi hóa khử được sắp xếp trong dãy điện hóa sau :
Fe2+/Fe ; Cu2+/Cu ; Fe3+/Fe2+
Theo qui luật biến đổi tính oxi hóa và khử của các chất và ion trong dãy thì :
Tính khử : Fe > Cu > Fe2+
Tính oxi hóa : Fe3+ > Cu2+ > Fe2+
Đáp án D
Đáp án A:
Tính khử : Fe > Fe2+ > Cu
Đáp án B:
Tính khử : Fe2+ > Cu > Fe
Đáp án C:
Tính oxi hóa : Cu2+ > Fe3+ > Fe2+
Đáp án D:
Tính oxi hóa : Fe3+> Cu2+ > Fe2+
Câu hỏi 11
Đáp án đúng:
Đáp án C
Câu hỏi:
Cho hỗn hợp chất rắn X gồm Al, Zn và Fe vào dung dịch CuCl2. Sau khi phản ứng xong được hỗn hợp rắn Y và dd Z. Thêm dung dịch NaOH dư vào dung dịch Z thấy xuất hiện kết tủa T. Vậy rắn Y có thể gồm:
Lời giải chi tiết :
\({\rm{ran}}\left\{ {{\rm{Al ; Zn va Fe}}\buildrel {{\rm{ + CuC}}{{\rm{l}}_{\rm{2}}}} \over\longrightarrow } \right.\matrix{
{{\rm{ddZ:A}}{{\rm{l}}^{{\rm{3 + }}}}{\rm{;Z}}{{\rm{n}}^{{\rm{2 + }}}}{\rm{;F}}{{\rm{e}}^{{\rm{2 + }}}}\buildrel { + NaOH\,du} \over\longrightarrow Fe{{(OH)}_2} \downarrow } \cr {{\rm{ranY: Fe; Cu}}} \cr} \)
Đáp án C
Đáp án A:
Zn, Fe, Cu
Đáp án B:
Al, Zn, Fe, Cu
Đáp án C:
Fe, Cu
Đáp án D:
Zn, Cu
Câu hỏi 12
Đáp án đúng:
Đáp án B
Câu hỏi:
Cho biết thứ tự từ trái sang phải của các cặp oxi hóa – khử trong dãy điện hóa như sau: Zn2+/Zn; Fe2+/Fe; Cu2+/ Cu; Fe3+/Fe2+; Ag+/Ag. Các kim loại và ion đều phản ứng được với ion Fe2+ trong dung dịch là
Lời giải chi tiết :
Đáp án B
Đáp án A:
Ag, Fe3+.
Đáp án B:
Zn, Ag+.
Đáp án C:
Ag, Cu2+.
Đáp án D:
Zn, Cu2+.
Câu hỏi 13
Đáp án đúng:
Đáp án C
Câu hỏi:
Hỗn hợp 1,3 mol Mg và x mol Zn vào dung dịch chứa 2 mol Cu2+ và 2 mol Ag+ sau phản ứng hoàn toàn, lọc bỏ phần dung dịch thu được chất rắn gồm 2 kim loại. Gía trị của x có thể là
Phương pháp giải :
Bảo toàn electron
Lời giải chi tiết :
Hỗn hợp thu được gồm 2 kim loại là Cu và Ag
Bảo toàn e: ne( Cu2+; Ag+ nhận) > n e (Mg, Zn nhường)
=> 2.2 + 2.1 > 1,3.2 + x.2
=> x < 1,7 mol
Đáp án C
Đáp án A:
2,0
Đáp án B:
2,2
Đáp án C:
1,5
Đáp án D:
1,8
Câu hỏi 14
Đáp án đúng:
Đáp án D
Câu hỏi:
Trong các ion sau: Ag+, Cu2+, Fe2+, Au3+, ion có tính oxi hóa mạnh nhất là
Lời giải chi tiết :
Ghi nhớ: Kim loại có tính khử càng yếu thì cation của nó có tính oxi hóa càng mạnh
Tính oxi hóa: Fe2+ < Cu 2+ < Ag+ < Au3+ => Au 3+ có tính oxi hóa mạnh nhất
Đáp án D
Đáp án A:
Fe2+
Đáp án B:
Cu2+
Đáp án C:
Ag+
Đáp án D:
Au3+
Câu hỏi 15
Đáp án đúng:
Đáp án D
Câu hỏi:
Trong phản ứng : $Cu + 2AgN{O_3} \to Cu(N{O_3}) + 2Ag$ . Phát biểu đúng là:
Lời giải chi tiết :
Đáp án D
Đáp án A:
Ion Cu2+ bị khử thành Cu.
Đáp án B:
Ion Ag+ bị oxi hóa thành Ag.
Đáp án C:
Cu bị khử thành Cu2+.
Đáp án D:
Ion Ag+ bị khử thành Ag.
Câu hỏi 16
Đáp án đúng:
Đáp án D
Câu hỏi:
Một tấm kim loại vàng bị bám một lớp Fe ở bề mặt. Ta có thể rửa lớp Fe để loại tạp chất bằng dung dịch nào?
Lời giải chi tiết :
Fe+2FeCl3 -> 3FeCl2
Đáp án D
Đáp án A:
Dung dịch ZnSO4 dư.
Đáp án B:
Dung dịch CuSO4 dư.
Đáp án C:
Dung dịch FeSO4 dư.
Đáp án D:
Dung dịch FeCl3
Câu hỏi 17
Đáp án đúng:
Đáp án D
Câu hỏi:
Cho Mg vào dung dịch FeSO4, và CuSO4. Sau phản ứng thu được chất rắn A gồm 2 kim loại và dung dịch B chứa 2 muối. Phản ứng kết thúc khi nào?
Lời giải chi tiết :
Hai kim loại là Cu, Fe
Hai muối là MgSO4, FeSO4 dư
Đáp án D
Đáp án A:
FeSO4 hết, CuSO4 hết và Mg hết.
Đáp án B:
FeSO4 hết, CuSO4 hết và Mg hết.
Đáp án C:
CuSO4 dư, FeSO4 chưa phản ứng, Mg hết .
Đáp án D:
CuSO4 dư, FeSO4 chưa phản ứng, Mg hết .
Câu hỏi 18
Đáp án đúng:
Đáp án D
Câu hỏi:
Hỗn hợp bột (chứa 2 chất có cùng số mol) nào sau đây không tan hết khi cho vào lượng dư dung dịch H2SO4 (loãng nóng, không có oxi) ?
Lời giải chi tiết :
Đáp án D
Đáp án A:
Fe3O4 và Cu
Đáp án B:
KNO3 và Cu
Đáp án C:
Fe và Zn
Đáp án D:
FeCl2 và Cu
Câu hỏi 19
Đáp án đúng:
Đáp án B
Câu hỏi:
Cho hỗn hợp gồm Zn và Fe vào dung dịch CuSO4, phản ứng xong thu được chất rắn X gồm 2 kim loại và dung dịch Y chứa 3 loại ion. Nhận xét nào sau đây là đúng
Lời giải chi tiết :
Thứ tự phản ứng :
Zn + Cu2+ → Zn2+ + Cu
Fe + Cu2+ → Fe2+ + Cu
=> chất rắn gồm 2 kim loại : Cu và Fe
Y chứa 3 ion là Zn2+ ; Fe2+ và SO42-.
=> Zn phản ứng hết, Fe còn dư, CuSO4 hết
Đáp án B
Đáp án A:
Zn chưa phản ứng hết, Fe chưa phản ứng, CuSO4 đã phản ứng hết
Đáp án B:
Zn đã phản ứng hết, Fe còn dư, CuSO4 đã phản ứng hết
Đáp án C:
Zn đã phản ứng hết, Fe phản ứng hết, CuSO4còn dư
Đáp án D:
Zn đã phản ứng hết, Fe chưa phản ứng, CuSO4 đã phản ứng hết
Câu hỏi 20
Đáp án đúng:
Đáp án A
Câu hỏi:
Hỗn hợp A gồm 2 kim loại Fe – Cu. Có thể dùng dung dịch nào sau đây để thu được Cu kim loại?
Lời giải chi tiết :
Dùng Cu(NO3)2 vì nó chỉ phản ứng với Fe tạo Cu kim loại
Đáp án A
Đáp án A:
Dung dịch Cu(NO3)2 dư
Đáp án B:
Dung dịch Fe(NO3)2 dư
Đáp án C:
Dung dịch FeCl3 dư
Câu hỏi 21
Đáp án đúng:
Đáp án B
Câu hỏi:
Cho hỗn hợp X gồm Al, Fe, Cu. Dung dịch nào sau đây khi lấy dư không thể hòa tan hết X :
Lời giải chi tiết :
Đáp án B
Đáp án A:
NaNO3 trong HCl
Đáp án B:
H2SO4 loãng
Đáp án C:
HNO3 loãng
Đáp án D:
H2SO4 đặc nóng
Câu hỏi 22
Đáp án đúng:
Đáp án B
Câu hỏi:
Hỗn hợp X gồm Al, Fe2O3 và Cu có số mol bằng nhau. Hỗn hợp X tan hoàn toàn trong dung dịch
Lời giải chi tiết :
- Gọi số mol mỗi chất trong X là 1 mol.
· Hòa tan X vào NaOH dư thì chỉ có Al tan trong Fe2O3 và Cu không tan. · Hòa tan X vào HCl dư:
Hỗn hợp tan hoàn toàn trong dung dịch HCl dư.
· Hòa tan X vào AgNO3 dư thì Al và Cu tan trong khi Fe2O3 không tan. · Hòa tan X vào NH3 (dư) thì không có chất nào tan. Chọn B
Đáp án A:
NaOH (dư)
Đáp án B:
HCl (dư)
Đáp án C:
AgNO3 (dư)
Đáp án D:
NH3 (dư)
Câu hỏi 23
Đáp án đúng:
Đáp án C
Câu hỏi:
Có một hỗn hợp gồm: Fe, Ag, Cu. Tách Ag ra khỏi hỗn hợp với khối lượng không đổi người ta dùng dung dịch
Lời giải chi tiết :
Ag không phản ứng được với dung dịch FeCl3
Đáp án C
Đáp án A:
AgNO3
Đáp án B:
Cu(NO3)2
Đáp án C:
FeCl3
Đáp án D:
FeCl2
Câu hỏi 24
Đáp án đúng:
Đáp án A
Câu hỏi:
Cho dãy các kim loại: Na, Al; Cu; Fe; Ag. Số kim loại tác dụng được với dung dịch Fe2(SO4)3 là:
Lời giải chi tiết :
Các kim loại tác dụng được dd với Fe2(SO4)3 là: Na, Al, Cu, Fe
Na + H2O → NaOH + H2↑
6NaOH + Fe2(SO4)3 → 2Fe(OH)3 ↓ + 3Na2SO4
Al + Fe2(SO4)3 → Al2(SO4)3 + Fe ↓
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
Fe + Fe2(SO4)3 → 3FeSO4
=> Có 4 kim loại tác dụng được với dd Fe2(SO4)3
Đáp án A
Đáp án A:
4
Đáp án B:
3
Đáp án C:
1
Đáp án D:
2
Câu hỏi 25
Đáp án đúng:
Đáp án A
Câu hỏi:
Ngâm thanh Cu dư vào dung dịch AgNO3 thu được dung dịch X. Sau đó ngâm thanh Fe dư vào dung dịch X thu được dung dịch Y. Biết các phản ứng xảy ra hoàn toàn. Dung dịch Y có chứa chất tan là:
Lời giải chi tiết :
\(Cu\,(du)\xrightarrow{{AgN{O_3}}}Cu{(N{O_3})_2}\xrightarrow{{Fe(du)}}Fe{(N{O_3})_2}\)
Đáp án A
Đáp án A:
Fe(NO3)2
Đáp án B:
Fe(NO3)2; Cu(NO3)2
Đáp án C:
Fe(NO3)3
Đáp án D:
Fe(NO3)3; Fe(NO3)2
Câu hỏi 26
Đáp án đúng:
Đáp án A
Câu hỏi:
Cho hỗn hợp Al, Fe tác dụng với hỗn hợp dung dịch AgNO3, Cu(NO3)2 thu được dung dịch B và chất rắn D gồm 3 kim loại. Cho D tác dụng với HCl dư, thấy có khí bay lên. Thành phần của chất rắn D là
Lời giải chi tiết :
Thứ tự phản ứng:
- Kim loại sẽ phản ứng theo thứ tự: Al, Fe
- Muối sẽ phản ứng theo thứ tự: AgNO3, Cu(NO3)2
Vậy 3 kim loại là: Fe, Ag, Cu
Đáp án A
Đáp án A:
Fe, Cu, Ag
Đáp án B:
Al, Cu, Ag
Đáp án C:
Al, Fe, Cu, Ag
Đáp án D:
Al, Fe, Cu
Câu hỏi 27
Đáp án đúng:
Đáp án B
Câu hỏi:
Cho các ion kim loại: Zn2+, Sn2+, Ni2+ , Fe2+, Pb2+ . Thứ tự tính oxh giảm dần là:
Lời giải chi tiết :
Đáp án B
Đáp án A:
Sn2+ > Ni2+ >Zn2+ > Pb2+ > Fe2+
Đáp án B:
Pb2+ > Sn2+ >Ni2+ >Fe2+ > Zn2+
Đáp án C:
Zn2+ > Sn2+ > Ni2+ > Fe2+ >Pb2+
Đáp án D:
Pb2+ > Sn2+ > Fe2+ > Ni2+ > Zn2+
Câu hỏi 28
Đáp án đúng:
Đáp án D
Câu hỏi:
Dùng hóa chất nào sau với HCl để nhận biết 4 kim loại K, Al, Ag, Fe ?
Lời giải chi tiết :
Dùng H2O
- Hòa tan các kim loại vào nước. Kim loại tan và sinh ra khí là K
- Lấy dung dịch thu được khi hòa tan K cho tác dụng với các dung dịch còn lại, kim loại nào phản ứng sinh ra khí là Al
- Cho 2 kim loại còn lại là Fe và Ag phản ứng với HCl, kim loại nào phản ứng với HCl sinh ra khí là Fe
Đáp án D
Đáp án A:
Chất rắn khan Ba(OH)2
Đáp án B:
Chất rắn khan NaOH
Đáp án C:
Dung dịch CuSO4
Đáp án D:
H2O
Câu hỏi 29
Đáp án đúng:
Đáp án A
Câu hỏi:
Cho cấu hình electron nguyên tử của 3 nguyên tố X, Y, Z lần lượt là: 1s22s22p63s2, 1s22s22p63s23p64s2, 1s22s22p63s23p1 . Nếu sắp xếp theo chiều tăng dần tính kim loại thì cách sắp xếp nào sau đây đúng
Phương pháp giải :
Đi theo chiều tăng của điện tích hạt nhân
Trong 1 chu kì: R giảm dần
Trong 1 nhóm: R tăng dần
Lời giải chi tiết :
Cấu hình electron nguyên tử của 3 nguyên tố X, Y, Z lần lượt là:
X: 1s22s22p63s2 => chu kì 3 nhóm IIA
Y: 1s22s22p63s23p64s2=>chu kì 4, nhóm IIA
Z: 1s22s22p63s23p1 => chu kì 3 nhóm IIIA
=> Bán kính: Y > X,Z
+ Cùng chu kì 3: bán kính của X>Z do ZX < ZZ
=>Bán kính: Z<X<Y =>
Đáp án A
Đáp án A:
Z < X < Y
Đáp án B:
Z < Y < X
Đáp án C:
Y < X < Z
Đáp án D:
K < Q < K
Câu hỏi 30
Đáp án đúng:
Đáp án A
Câu hỏi:
Cho 3 kim loại Cu, Fe, Al và 4 dung dịch CuSO4, AgNO3, CuCl2 và FeSO4. Kim loại nào sau đây khử được cả 4 dung dịch muối?
Phương pháp giải :
Trong dãy hoạt động hóa học của kim loại, kim loại đứng trước đẩy kim loại đứng sau ra khỏi muối của nó.
Lời giải chi tiết :
Al đứng trước Cu, Ag, Fe => Al khử được cả 4 dung dịch muối
Đáp án A
Đáp án A:
Al.
Đáp án B:
Tất cả đều sai.
Đáp án C:
Fe
Đáp án D:
Cu.
Câu hỏi 31
Đáp án đúng:
Đáp án A
Câu hỏi:
Cho phản ứng: Cu +Fe3+→Cu2+ + Fe2+
Lời giải chi tiết :
Đáp án A
Đáp án A:
Tính khử của Cu mạnh hơn Fe2+
Đáp án B:
Tính oxi hóa của ion Fe2+ mạnh hơn tính oxi hóa của Cu2+
Đáp án C:
Kim loại Cu đẩy được Fe ra khỏi muối
Đáp án D:
Tính oxi hóa của ion Cu2+ mạnh hơn tính oxi hóa của ion Fe3+
Câu hỏi 32
Đáp án đúng:
Đáp án B
Câu hỏi:
Hãy sắp xếp các ion Cu2+, Hg2+, Fe2+, Pb2+, Ca2+ theo chiều tính oxi hóa tăng dần?
Phương pháp giải :
Ghi nhớ: Kim loại có tính khử càng mạnh thì cation kim loại tương ứng của chúng có tính oxi hóa càng yếu và ngược lại
Lời giải chi tiết :
Tính oxi hóa tăng dần là: Ca2+ < Fe2+ < Pb2+ < Cu2+ < Hg2+.
Đáp án B
Đáp án A:
Hg2+ < Cu2+ < Pb2+ < Cu2+.
Đáp án B:
Ca2+ < Fe2+ < Pb2+ < Cu2+ < Hg2+.
Đáp án C:
Ca2+ < Fe2+ < Cu2+ < Pb2+ < Hg2+
Đáp án D:
Ca2+ < Fe2+ < Pb2+ < Cu2+.
Câu hỏi 33
Đáp án đúng:
Đáp án A
Câu hỏi:
Cho phản ứng hóa học: Mg + CuSO4 → MgSO4 + Cu
Quá trình nào dưới đây biểu thị sự oxi hóa của phản ứng trên:
Phương pháp giải :
Ghi nhớ: quá trình oxi hóa là quá trình nhường electron, số oxi hóa của chất sau phản ứng tăng lên
Lời giải chi tiết :
\(\mathop {Mg}\limits^0 + \mathop {Cu}\limits^{ + 2} S{O_4}\xrightarrow{{}}\mathop {Mg}\limits^{ + 2} S{O_4} + \mathop {Cu}\limits^0 \downarrow \)
=> Mg có số oxi hóa tăng sau phản ứng => quá trình oxi hóa Mg là: Mg → Mg2+ + 2e.
Đáp án A
Đáp án A:
Mg → Mg2+ + 2e.
Đáp án B:
Cu → Cu2+ + 2e
Đáp án C:
Cu2+ + 2e → Cu
Đáp án D:
Mg2+ + 2e → Mg
Câu hỏi 34
Đáp án đúng:
Đáp án B
Câu hỏi:
Vị trí của một số cặp oxi hóa – khử theo chiều tính khử giảm dần từ trái sang phải được sắp xếp như sau: Fe2+/ Fe, Cu2+ / Cu, Fe3+/Fe2+, Ag+/ Ag, Cl2/Cl-
Trong các chất sau: Cu, AgNO3, Cl2. Chất nào tác dụng với dung dịch Fe(NO3)2.
Phương pháp giải :
Ghi nhớ: Quy tắc α
Chất khử mạnh + chất oxi hóa mạnh → chất khử yếu + chất oxi hóa yếu
Lời giải chi tiết :
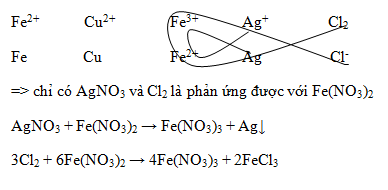
Đáp án B
Đáp án A:
AgNO3.
Đáp án B:
AgNO3, Cl2.
Đáp án C:
Cả 3 chất.
Đáp án D:
Cl2.
Câu hỏi 35
Đáp án đúng:
Đáp án C
Câu hỏi:
Cho các phản ứng sau:
(1) X + X3+ → X2+
(2) X2+ + Y+ → X3+ + Y
Sự sắp xếp đúng với chiều tăng dần tính oxi hóa của các cation là
Lời giải chi tiết :
(1) X3+ có tính oxi hóa mạnh hơn X2+
(2) Y+ có tính oxi hóa mạnh hơn X3+
Vậy tính oxi hóa X2+ < X3+ < Y+
Đáp án C
Đáp án A:
X3+, X2+, Y+.
Đáp án B:
X2+, Y+, X3+.
Đáp án C:
X2+, X3+, Y+.
Đáp án D:
Y+, X2+, X3+.
Câu hỏi 36
Đáp án đúng:
Đáp án B
Câu hỏi:
Cho dãy các kim loại sau : Ni, Fe, Zn, Na, Cu, Al, Ag. Số kim loại trong dãy khử được ion Fe3+ trong dung dịch muối là
Lời giải chi tiết :
Cho dãy các kim loại sau :, Na, , Ag.
Số kim loại trong dãy khử được ion Fe3+ trong dung dịch muối là Ni, Fe, Zn, Cu, Al
Chọn B
Đáp án A:
4
Đáp án B:
5
Đáp án C:
6
Đáp án D:
7
Câu hỏi 37
Đáp án đúng:
Đáp án C
Câu hỏi:
Để tách lấy Ag ra khỏi hỗn hợp gồm Fe, Cu, Ag ta dùng lượng dư dung dịch
Lời giải chi tiết :
Tách Ag ra khỏi hỗn hợp Fe, Cu, Ag => ta dùng Fe2(SO4)3 do Ag không tác dụng, còn Fe và Cu tác dụng được
Fe + Fe2(SO4)3 → 3FeSO4
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
Đáp án C
Đáp án A:
NaOH.
Đáp án B:
HCl.
Đáp án C:
Fe2(SO4)3.
Đáp án D:
HNO3.
Câu hỏi 38
Đáp án đúng:
Đáp án D
Câu hỏi:
Kim loại Ni phản ứng được với tất cả các muối trong dung dịch của dãy nào sau đây?
Phương pháp giải :
KL mạnh có thể phản ứng được với muối của KL yếu hơn
Lời giải chi tiết :
Ni có thể phản ứng được với muối của KL yếu hơn
A loại NaCl, AlCl3, ZnCl2
B loại NaCl
C loại MgSO4
D thỏa mãn
Đáp án D
Đáp án A:
NaCl, AlCl3, ZnCl2.
Đáp án B:
Pb(NO3)2, AgNO3, NaCl.
Đáp án C:
MgSO4, CuSO4, AgNO3.
Đáp án D:
AgNO3, CuSO4, Pb(NO3)2.
Câu hỏi 39
Đáp án đúng:
Đáp án B
Câu hỏi:
Cho các ion sau: Al3+, Fe2+, Cu2+, Ag+, Ca2+. Chiều giảm tính oxi hóa của các ion trên là
Phương pháp giải :
Dãy điện hóa được sắp xếp theo chiều tính khử của các KL giảm dần và tính oxi hóa của các ion tăng dần
Lời giải chi tiết :
Dãy điện hóa được sắp xếp theo chiều tính khử của các KL giảm dần và tính oxi hóa của các ion tăng dần
Do đó ta có sự sắp xếp tính oxi hóa: Ag+ > Cu2+ > Fe2+ > Al3+ > Ca2+
Đáp án B
Đáp án A:
Ca2+, Fe2+, Al3+, Cu2+, Ag+.
Đáp án B:
Ag+, Cu2+, Fe2+, Al3+, Ca2+.
Đáp án C:
Cu2+, Ag+, Fe2+, Al3+, Ca2+.
Đáp án D:
Ca2+, Al3+, Fe2+, Cu2+, Ag+.
Câu hỏi 40
Đáp án đúng:
Đáp án B
Câu hỏi:
Cho các phản ứng sau:
X + 2X(NO3)3 → 3X(NO3)2
YNO3 + X(NO3)2 → X(NO3)3 + Y
Dãy sắp xếp theo thứ tự tăng dần tính oxi hóa các ion kim loại là:
Phương pháp giải :
Phản ứng hóa học xảy ra theo chiều tạo ra các chất có tính khử và tính oxi hóa yếu hơn chất tham gia phản ứng.
Lời giải chi tiết :
Phản ứng (1) => X3+ có tính oxi hóa mạnh hơn X2+
Phản ứng (2) => Y+ có tính oxi hóa mạnh hơn X3+
Vậy tính oxi hóa: X2+< X3+< Y+
Đáp án B
Đáp án A:
X2+, Y+, X3+.
Đáp án B:
X2+, X3+, Y+.
Đáp án C:
Y+, X2+, X3+.
Đáp án D:
Y+, X3+, Y2+.
Câu hỏi 41
Đáp án đúng:
Đáp án A
Câu hỏi:
Cho các cặp oxi hóa – khử được sắp xếp theo chiều tăng dần tính oxi hóa của dạng oxi hóa như sau:
Fe2+/Fe, Cu2+/Cu, Fe3+/Fe2+. Có các phát biểu sau:
a) Cu khử được Fe3+ thành Fe.
b) Cu2+ oxi hóa được Fe2+ thành Fe3+.
c) Fe3+ oxi hóa được Cu thành Cu2+.
d) Fe2+ oxi hóa được Cu thành Cu2+.
Số phát biểu đúng là:
Phương pháp giải :
Dựa vào dãy điện hóa (quy tắc α)
Lời giải chi tiết :
a) Sai vì Cu chỉ khử được Fe3+ thành Fe2+
b) Sai vì không có phản ứng
c) Đúng
d) Sai vì không có phản ứng
Đáp án A
Đáp án A:
1
Đáp án B:
3
Đáp án C:
4
Đáp án D:
2
Câu hỏi 42
Đáp án đúng:
Đáp án B
Câu hỏi:
Tiến hành các thí nghiệm sau :
(1) Nhúng thanh Fe vào dung dịch H2SO4 loãng
(2) Nhúng thanh Fe vào dung dịch H2SO4 loãng có thêm CuCl2
(3) Nhúng thanh Cu vào dung dịch FeCl3
(4) Nhúng thanh Fe vào dung dịch Fe2(SO4)3
Số thí nghiệm có sự ăn mòn điện hóa là :
Phương pháp giải :
Điều kiện để có ăn mòn điện hóa :
+) 2 điện cực khác bản chất (KL-KL, KL-PK, …)
+) 2 điện cực cùng nhúng vào dung dịch điện ly
+) 2 điện cực nối với nhau bằng dây dẫn hoặc tiếp xúc trực tiếp với nhau
Lời giải chi tiết :
=> Các thí nghiệm thỏa mãn : (2)
Đáp án B
Đáp án A:
3
Đáp án B:
1
Đáp án C:
2
Đáp án D:
4
Câu hỏi 43
Đáp án đúng:
Đáp án C
Câu hỏi:
Cho hỗn hợp gồm Fe và Mg vào dung dịch AgNO3, khi các phản ứng xảy ra hoàn toàn thu được dung dịch X (gồm hai muối) và chất rắn Y (gồm hai kim loại). Hai muối trong X là
Phương pháp giải :
Thứ tự phản ứng là: Mg, Fe
Lời giải chi tiết :
2 kim loại sau phản ứng là: Ag và Fe dư
=> AgNO3 phản ứng hết nên không có phản ứng: AgNO3 + Fe(NO3)2 → Fe(NO3)3 + Ag↓
Vậy 2 muối là: Mg(NO3)2 và Fe(NO3)2
Đáp án C
Đáp án A:
Fe(NO3)2 và AgNO3
Đáp án B:
Fe(NO3)3 và Mg(NO3)2
Đáp án C:
Mg(NO3)2 và Fe(NO3)2
Đáp án D:
AgNO3 và Mg(NO3)2
Câu hỏi 44
Đáp án đúng:
Đáp án C
Câu hỏi:
Cho thứ tự một số cặp oxi hóa khử trong dãy điện hóa như sau:
\(\frac{{A{l^{3 + }}}}{{Al}};\frac{{Z{n^{2 + }}}}{{Zn}};\frac{{F{{\rm{e}}^{2 + }}}}{{F{\rm{e}}}};\frac{{C{u^{2 + }}}}{{Cu}};\frac{{F{{\rm{e}}^{3 + }}}}{{F{{\rm{e}}^{{\rm{2 + }}}}}};\frac{{A{g^ + }}}{{Ag}}\)
Trong số các kim loại Al, Fe, Zn, Cu, Ag thì số kim loại có phản ứng trong dung dịch Fe(NO3)3 là
Phương pháp giải :
Dựa vào quy tắc α.
Lời giải chi tiết :
Các kim loại phản ứng được với dung dịch Fe(NO3)3 là: Al, Fe, Zn, Cu.
Đáp án C
Đáp án A:
5
Đáp án B:
3
Đáp án C:
4
Đáp án D:
2
Câu hỏi 45
Đáp án đúng:
Đáp án B
Câu hỏi:
Cho hỗn hợp bột gồm Al, Cu vào dung dịch chứa AgNO3 và Fe(NO3)3, sau phản ứng hoàn toàn thu được chất rắn X gồm hai kim loại và dung dịch Y chứa ba muối. Các cation trong dung dịch Y là
Lời giải chi tiết :
Vì sản phẩm gồm 2 kim loại => chắc chắn đó là : Ag và Cu
Mà Cu dư thì Fe(NO3)3 phải hết.
Dung dịch chứa các muối : Al3+ ; Fe2+ ; Cu2+
Các phản ứng :
Al + 3AgNO3 -> Al(NO3)3 + 3Ag
Al + 2Fe(NO3)3 -> Al(NO3)3 + Fe(NO3)2
Cu + 2AgNO3 -> Cu(NO3)2 + 2Ag
Cu + 2Fe(NO3)3 -> Cu(NO3)2 + 2Fe(NO3)2
Đáp án B
Đáp án A:
Fe3+, Ag+, Cu2+.
Đáp án B:
Al3+, Fe2+, Cu2+.
Đáp án C:
Al3+, Fe3+, Cu2+.
Đáp án D:
Al3+, Fe3+, Fe2+.
Câu hỏi 46
Đáp án đúng:
Đáp án A
Câu hỏi:
Cho dãy kim loại sau: K, Ca, Cu, Al, Zn, Ni, Fe, Ag, Mg, Cr, Au, Pb. Số kim loại vừa tác dụng được với dung dịch HCl và vừa tác dụng với HNO3 đặc nguội là
Phương pháp giải :
- Tác dụng với HCl: Những kim loại đứng trước H trong dãy hoạt động hóa học
- Những kim loại bị thụ động (hiểu đơn giản là không phản ứng) với axit HNO3 đặc nguội và H2SO4 đặc nguội: Al, Fe, Cr
Lời giải chi tiết :
- Những KL tác dụng với HCl: K, Ca, Al, Zn, Ni, Fe, Mg, Cr, Pb.
- Những KL tác dụng với HNO3 đặc nguội: K, Ca, Cu, Zn, Ni, Ag, Mg, Pb.
Như vậy các chất vừa tác dụng với HCl và HNO3 đặc nguội là: K, Ca, Zn, Ni, Mg, Pb.
Đáp án A
Đáp án A:
6
Đáp án B:
7
Đáp án C:
8
Đáp án D:
9
Câu hỏi 47
Đáp án đúng:
Đáp án D
Câu hỏi:
Cho phương trình phản ứng aAl +bHNO3 → cAl(NO3)3 + dNO + eH2O.Tỉ lệ a: b là
Phương pháp giải :
Cân bằng phương trình theo phương pháp thăng bằng electron
Lời giải chi tiết :
\(\begin{array}{l}
1x(\mathop {Al}\limits^0 \to \mathop {Al}\limits^{ + 3} + 3e)\\
1x(\mathop N\limits^{ + 5} + 3e \to \mathop N\limits^{ + 2} )
\end{array}\)
Al + 4HNO3 → Al(NO3)3 + NO + 2H2O
Vậy a: b = 1: 4
Đáp án D
Đáp án A:
1 : 3
Đáp án B:
2 : 3
Đáp án C:
2 : 5
Đáp án D:
1 : 4
Câu hỏi 48
Đáp án đúng:
Đáp án C
Câu hỏi:
Kim loại sắt không phản ứng được với dung dịch nào sau đây?
Phương pháp giải :
Các kim loại Fe, Al, Cr không phản ứng với HNO3 đặc nguội và H2SO4 đặc nguội do bị thụ động hóa trong các axit này.
Giải thích thêm về hiện tượng thụ động hóa: hiện tượng này là hiện tượng làm mất khả năng phản ứng của các chất.
VD: Khi cho Fe vào HNO3 đặc nguội hoặc H2SO4 đặc nguội sau đó cho vào dd HCl thì Fe không phản ứng được với HCl nữa.
Lời giải chi tiết :
Kim loại sắt không phản ứng với HNO3 đặc nguội và H2SO4 đặc nguội do bị thụ động hóa trong các axit này.
Giải thích thêm về hiện tượng thụ động hóa: hiện tượng này là hiện tượng làm mất khả năng phản ứng của các chất.
VD: Khi cho Fe vào HNO3 đặc nguội hoặc H2SO4 đặc nguội sau đó cho vào dd HCl thì Fe không phản ứng được với HCl nữa.
Đáp án C
Đáp án A:
H2SO4 loãng
Đáp án B:
HNO3 loãng
Đáp án C:
HNO3 đặc, nguội
Đáp án D:
H2SO4 đặc nóng
Câu hỏi 49
Đáp án đúng:
Đáp án B
Câu hỏi:
Cho các phản ứng sau:
Fe + 2Fe(NO3)3 → 3Fe(NO3)2;
AgNO3 + Fe(NO3)2 → Fe(NO3)3 + Ag
Dãy sắp xếp theo thứ tự tăng dần tính oxi hóa các ion kim loại là:
Phương pháp giải :
Từ phản ứng xảy ra ta suy ra tính oxi hóa của các ion kim loại theo quy tắc α
Lời giải chi tiết :
Fe + 2Fe(NO3)3 → 3Fe(NO3)2
→ Tính oxi hóa của Fe3+ > Fe2+
AgNO3 + Fe(NO3)2 → Fe(NO3)3 + Ag
→ Tính oxi hóa của Ag+ > Fe3+
Vậy tính oxi hóa của Ag+ > Fe3+ > Fe2+
Dãy sắp xếp theo thứ tự tăng dần tính oxi hóa các ion kim loại là: Fe2+, Fe3+, Ag+
Đáp án B
Đáp án A:
Ag+, Fe2+, Fe3+
Đáp án B:
Fe2+, Fe3+, Ag+
Đáp án C:
Fe2+, Ag+, Fe3+
Đáp án D:
Ag+, Fe3+, Fe2+
Câu hỏi 50
Đáp án đúng:
Đáp án A
Câu hỏi:
Cho hỗn hợp 2 kim loại Al và Cu vào dung dịch hỗn hợp 2 muối AgNO3 và Ni(NO3)2. Kết thúc phản ứng được rắn X (tan một phần trong dung dịch HCl dư) và thu được dung dịch Y (phản ứng vừa đủ với dung dịch NaOH được tủa gồm 2 hydroxit kim loại). Nhận xét nào sau đây không đúng về thí nghiệm trên
Lời giải chi tiết :
Đầu tiên Al phản ứng với AgNO3 trước
(1) Nếu Al còn dư thì phản ứng với Ni(NO3)2 ; Cu không phản ứng
(2) Nếu Al hết và AgNO3 dư thì Cu phản ứng với AgNO3 , Ni(NO3)2 giừ nguyên.
X tan 1 phần trong HCl => Chứng tỏ giả thuyết (1) đúng
=> Y gồm Al3+ ; Ni2+ ( có thể )
Mà Y phản ứng với NaOH vừa đủ tạo 2 hydroxit => Y phải có Ni2+
=> Rắn X gồm Ag, Cu , Ni
Đáp án A
Đáp án A:
Rắn X gồm Ag ,Al , Cu
Đáp án B:
Kim loại Cu chưa tham gia phản ứng
Đáp án C:
Dung dịch Ygồm Al(NO3)3,Ni(NO3)2
Đáp án D:
Rắn X gồm Ag,Cu và Ni


