Lý thuyết và bài tập cho Bài 2. Hạt nhân nguyên tử, nguyên tố hoá học, đồng vị, chương 1, Hóa lớp 10
Phương pháp giải một số bài toán ngắn gọn, dễ hiểu.
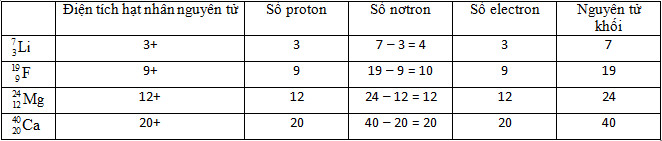
Dạng 1: Xác định A, Z trong nguyên tử và kí hiệu nguyên tử nguyên tố hóa học
Lý thuyết cần nhớ:
- Nguyên tử trung hoà về điện nên số proton trong hạt nhân bằng số electron của nguyên
Số đơn vị điện tích hạt nhân Z = số proton = số electron
Bài Tập / Bài Soạn:


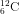 chiếm 98,89% và
chiếm 98,89% và 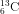 chiếm 1,11%.
chiếm 1,11%.